[最も選択された] 砂糖 の ���解度 897307

中学受験理科講座 水溶液の濃さと溶解度
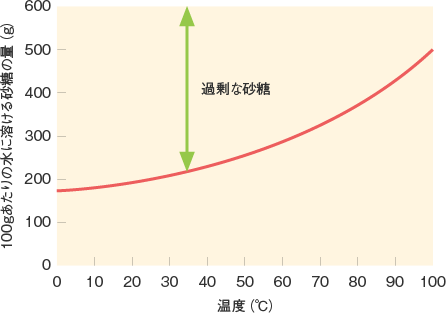
塩化ナトリウムの水に対する溶解熱は 3kJ/mol (吸熱) です。 砂糖=ショ糖(スクロース)の溶解熱のデーターが見つからないのですが、溶解度の温度変化から逆算すると、 約43kJ/mol (吸3 rows ちなみに、例えば100℃で487g溶ける砂糖の飽和水溶液の温度が下がると、溶解度は温度と共に減って、また物質が現れます。これを 結晶といいます。 問題を解いてみましょう!
砂糖 の 溶解度
砂糖 の 溶解度- 砂糖の糖度は、ショ糖の「旋光性」という性質を利用し、「旋光糖度計」という計測器で測り、単位 Z °で示します。 「旋光性」とは、光を通したときに波のように揺れる光の振動面そんなに大変な実験はできそうにないな、ということで溶解度の実験にしました。 これなら簡単です! うん、使うのは身近な調味料にしよう。塩と砂糖、これでレッツゴー! そうと決まれば実際に実

理科年表オフィシャルサイト 物理 化学部 有機物の水に対する溶解度
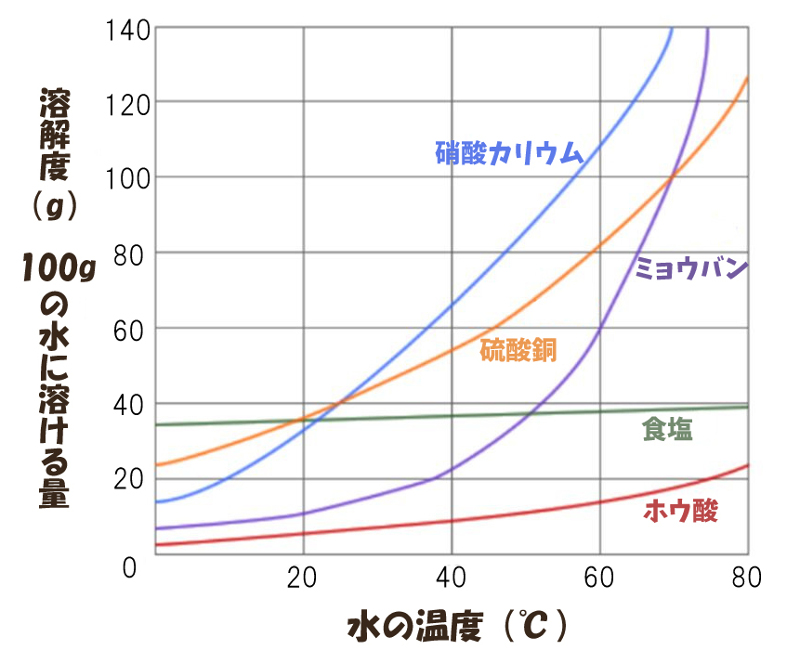
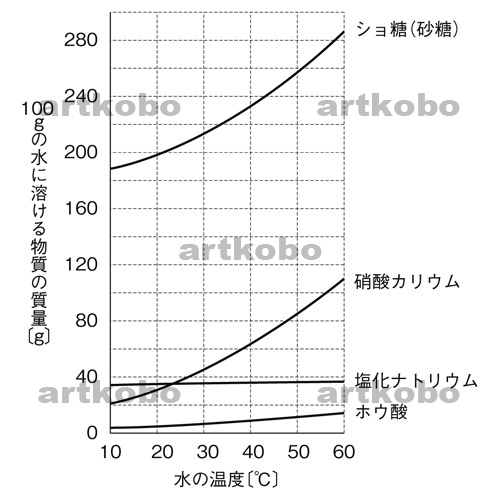
実験3-1 水溶液中での再結晶 高温ほど溶解度の差が大きいことを利用する。 実験3-2 エタノール水溶液中での再結晶 エタノールを用いて溶液の粘度や溶解度を調節する。 実験3-3 氷砂糖を用いそして、水100gにほう和する溶質の重さを 溶解度 とします。 温度による溶解度のちがい 固体が水に溶ける場合 基本的に水の温度が高くなるほど溶解度は大きくなります。冷たい紅茶では角砂糖(固4.製作方法 (1)砂糖液を作る 例:1リットル程度のガラス容器を準備し,水250cm 3 に砂糖700g程度を用いる。 「 100cm 3 の水に対し,砂糖を250~300g程度の比率」 結晶を作る容器の大きさ
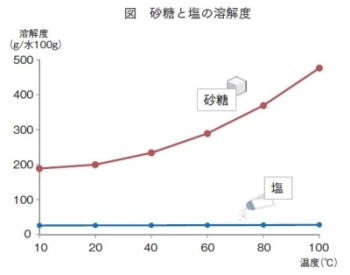
砂糖の調理性 (1)砂糖の高親水性・高溶解性・脱水作用 砂糖は、℃の水100gに約0g、100℃の湯に約476g溶解する。 溶解性の高い砂糖は食品中で水を強く引きつけ、その食品を水に ただし、水は100gに対して砂糖の溶解度は0℃で180g、 ℃で、4g、100℃で487gとして計算すること。 以上の問題が、分かりません。 わかる方教えてください質の溶解度を質量モル濃度で表すと , 気体分圧が1 atm の ときに,ヘ ン リーの法則が成立するような溶 解度の小さい気体では , 水に溶解しやすい 固体物質に 比べて,約1/1000から1/100程度
砂糖 の 溶解度のギャラリー
各画像をクリックすると、ダウンロードまたは拡大表示できます
 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 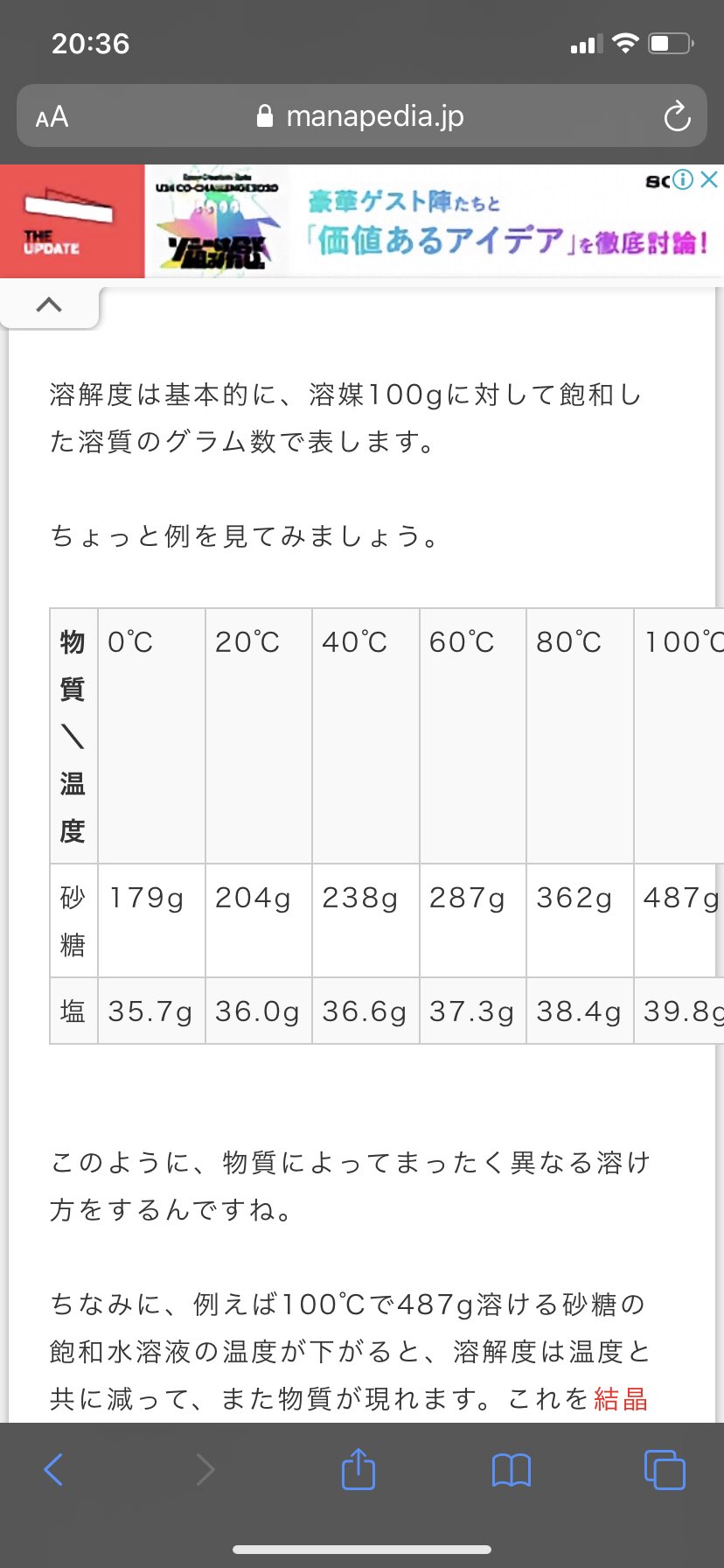 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 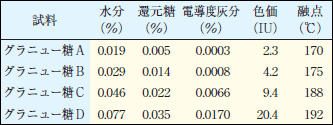 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 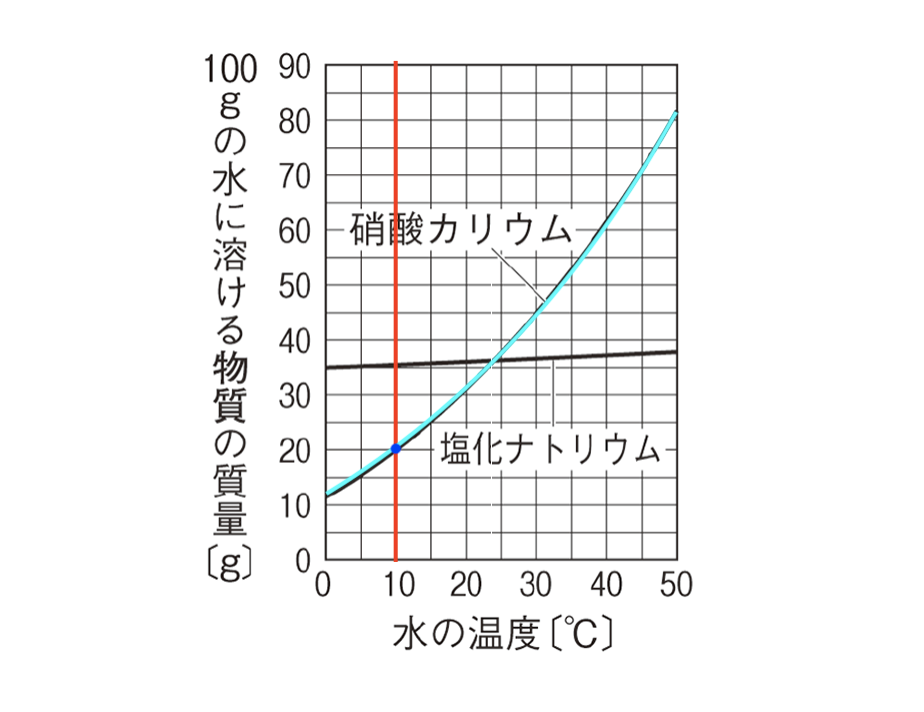 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 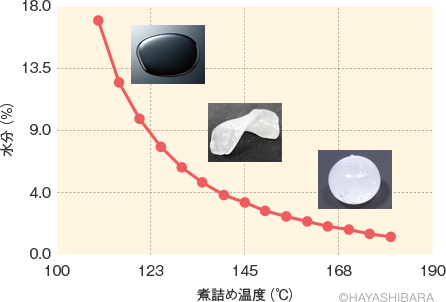 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 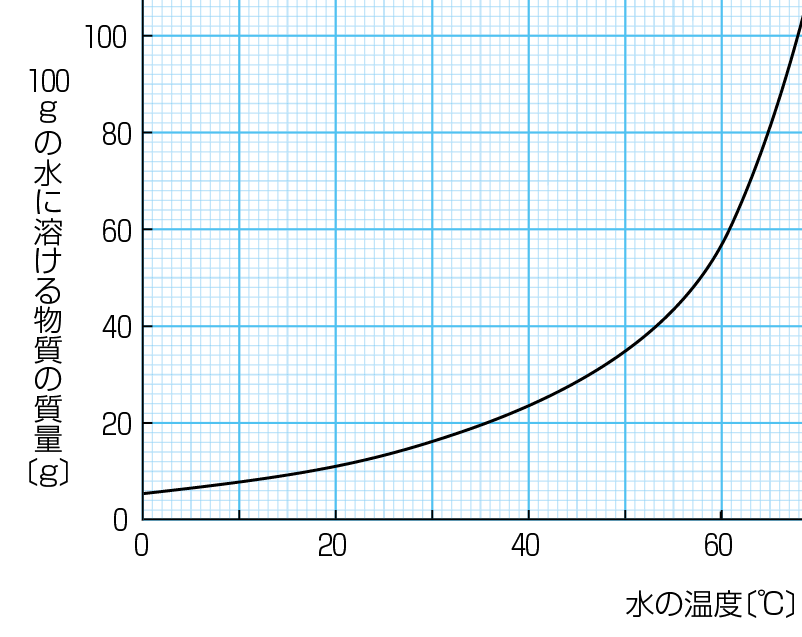 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 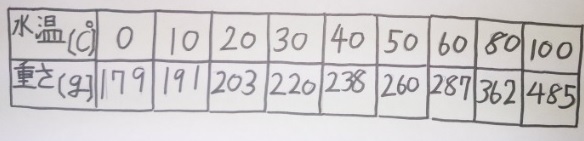 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 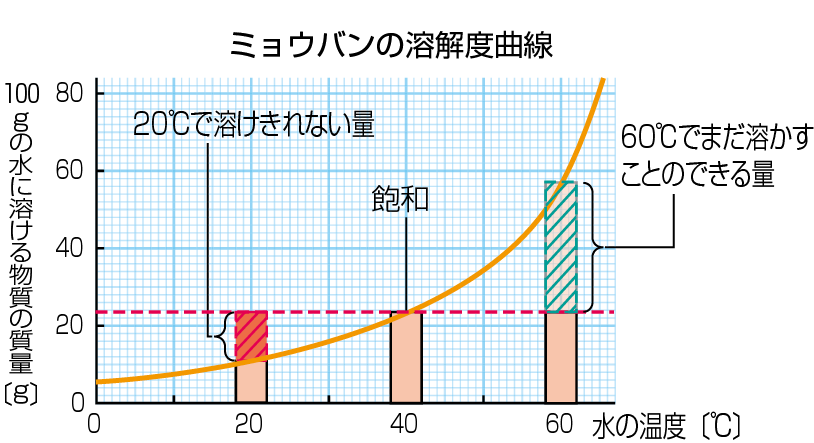 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 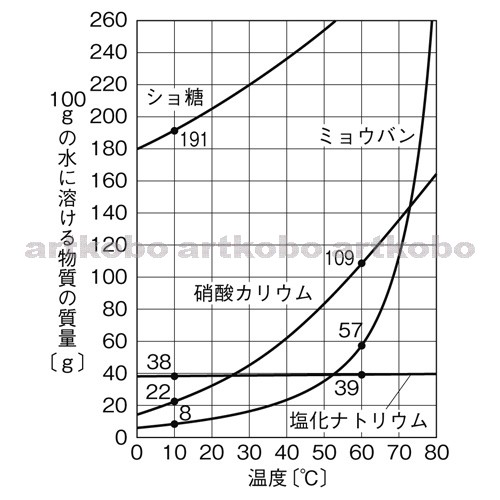 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 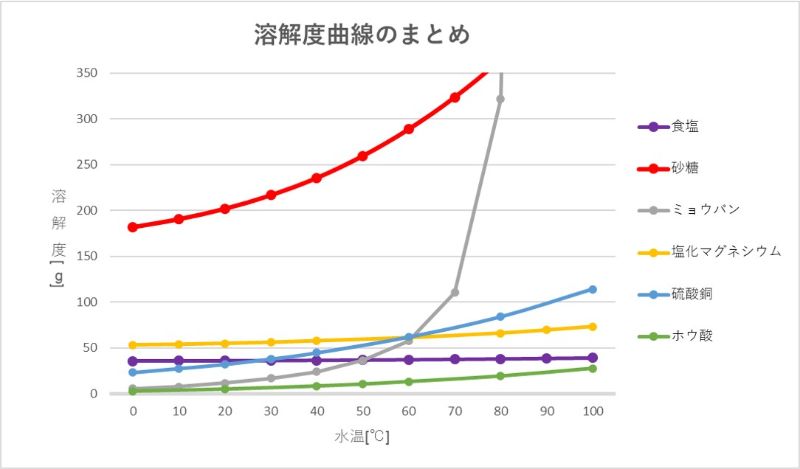 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 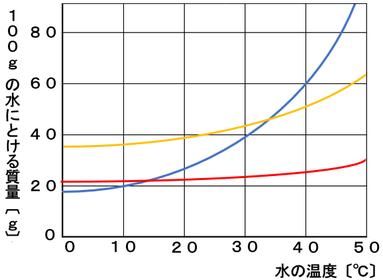 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 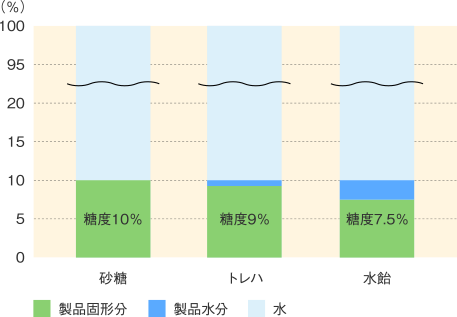 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 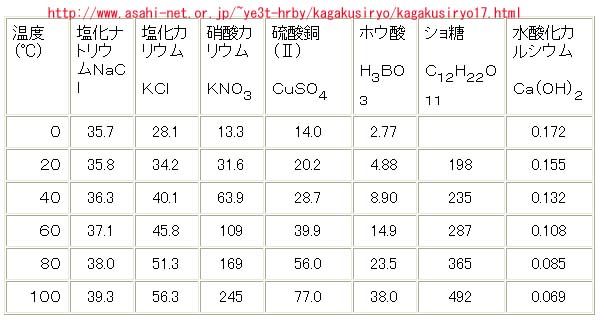 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 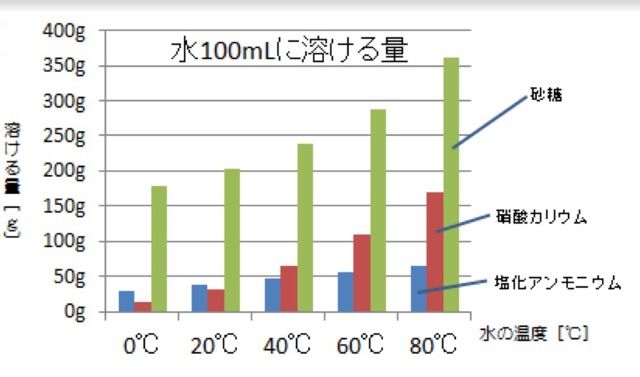 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 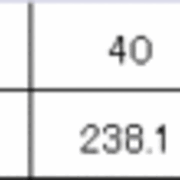 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 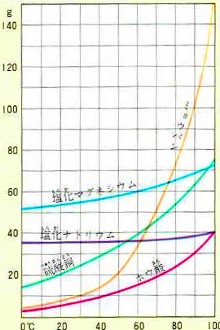 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 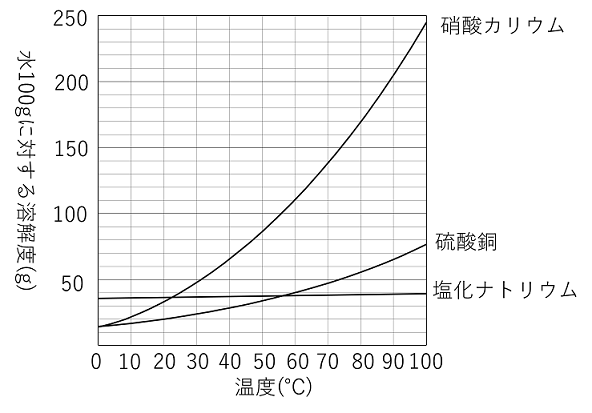 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 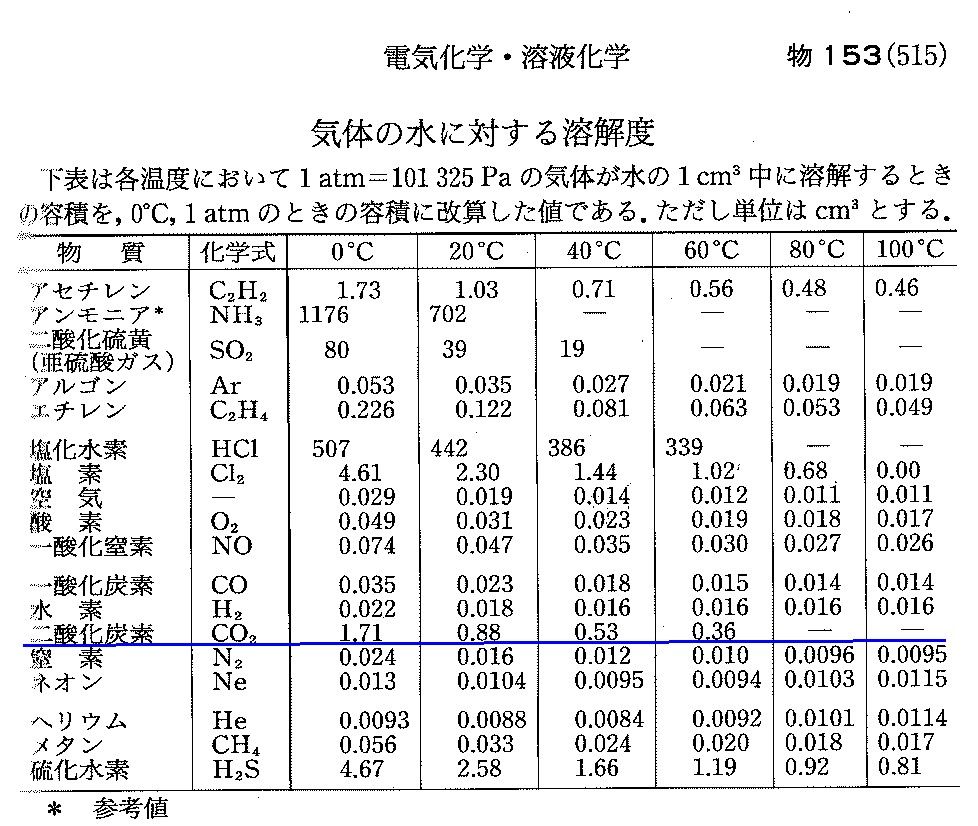 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 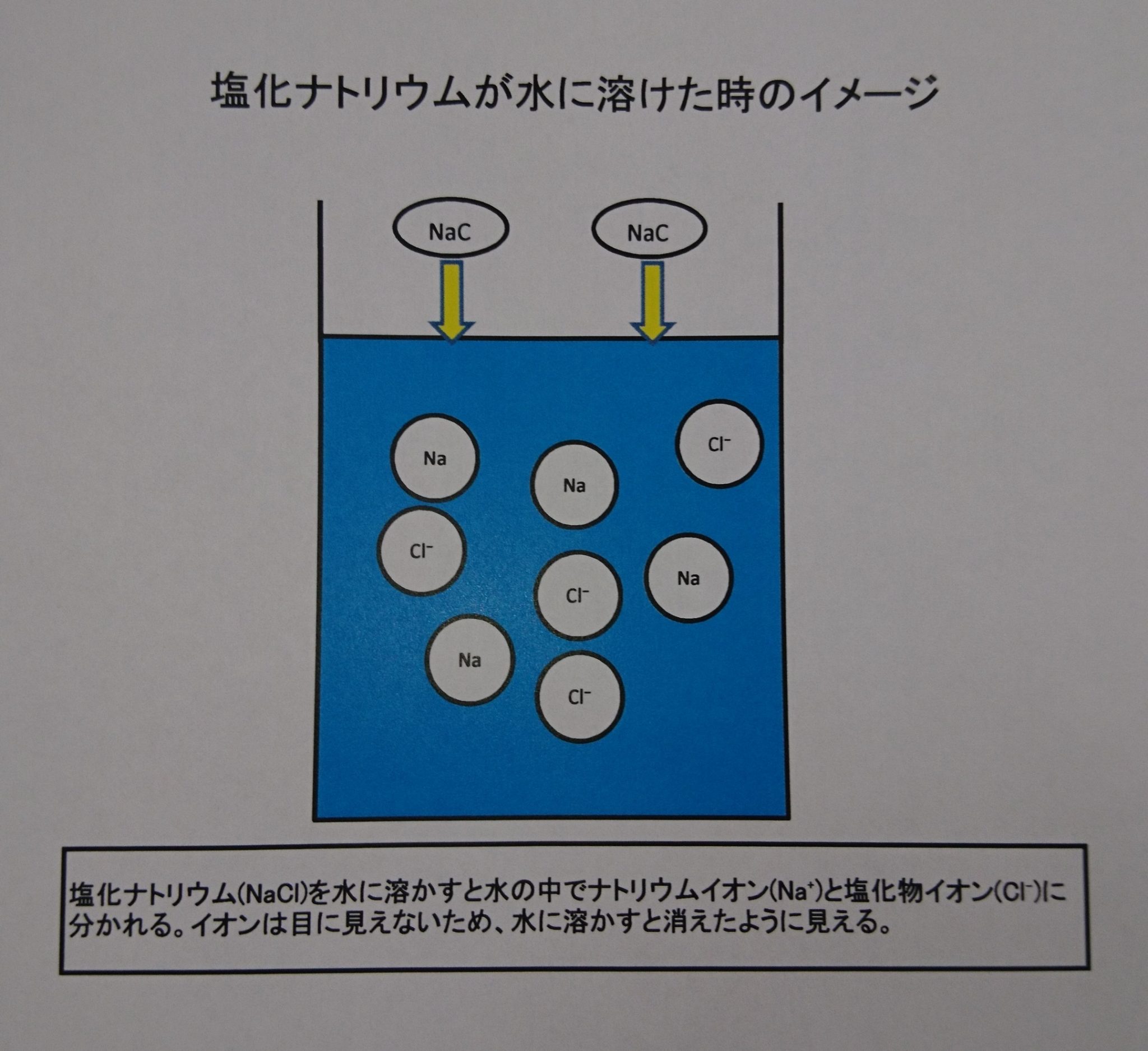 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 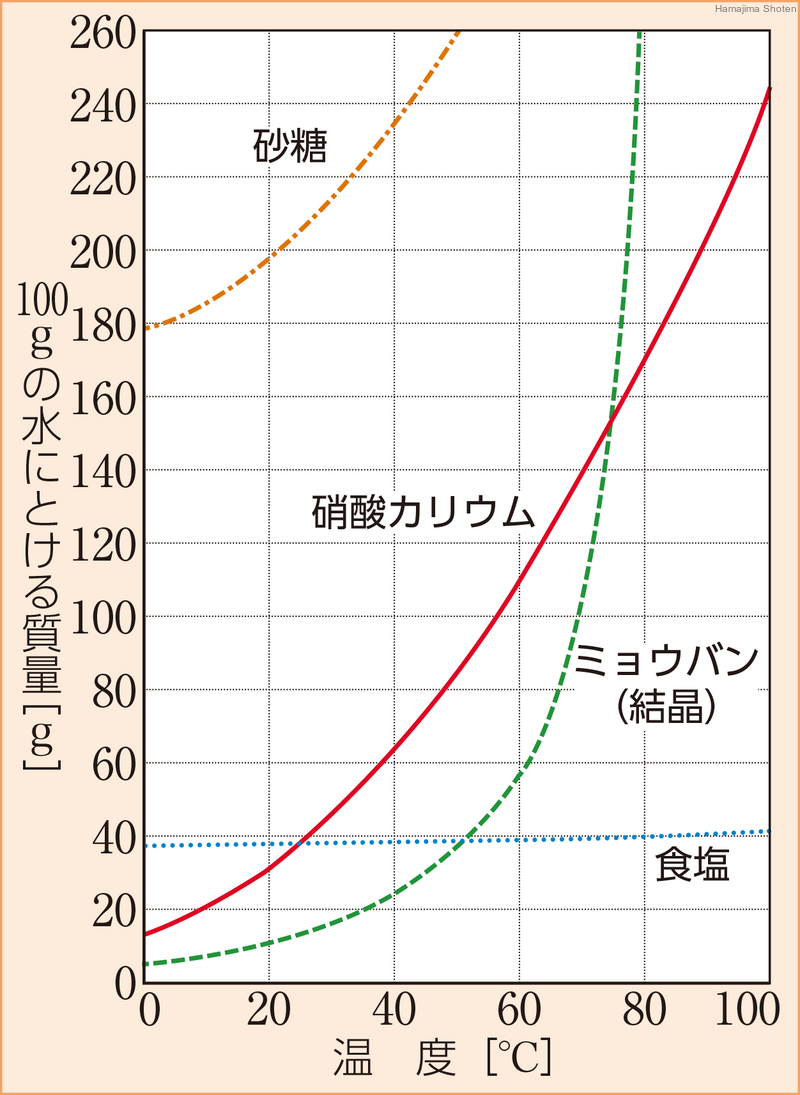 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 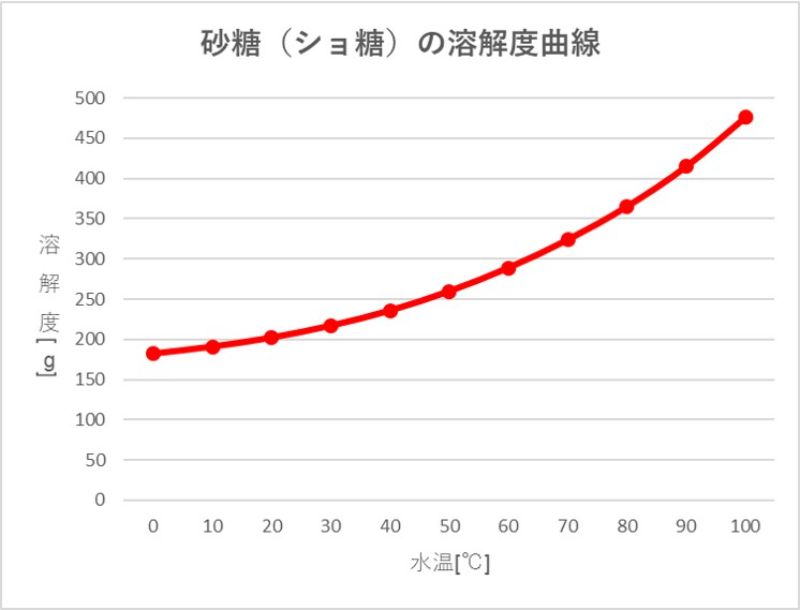 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 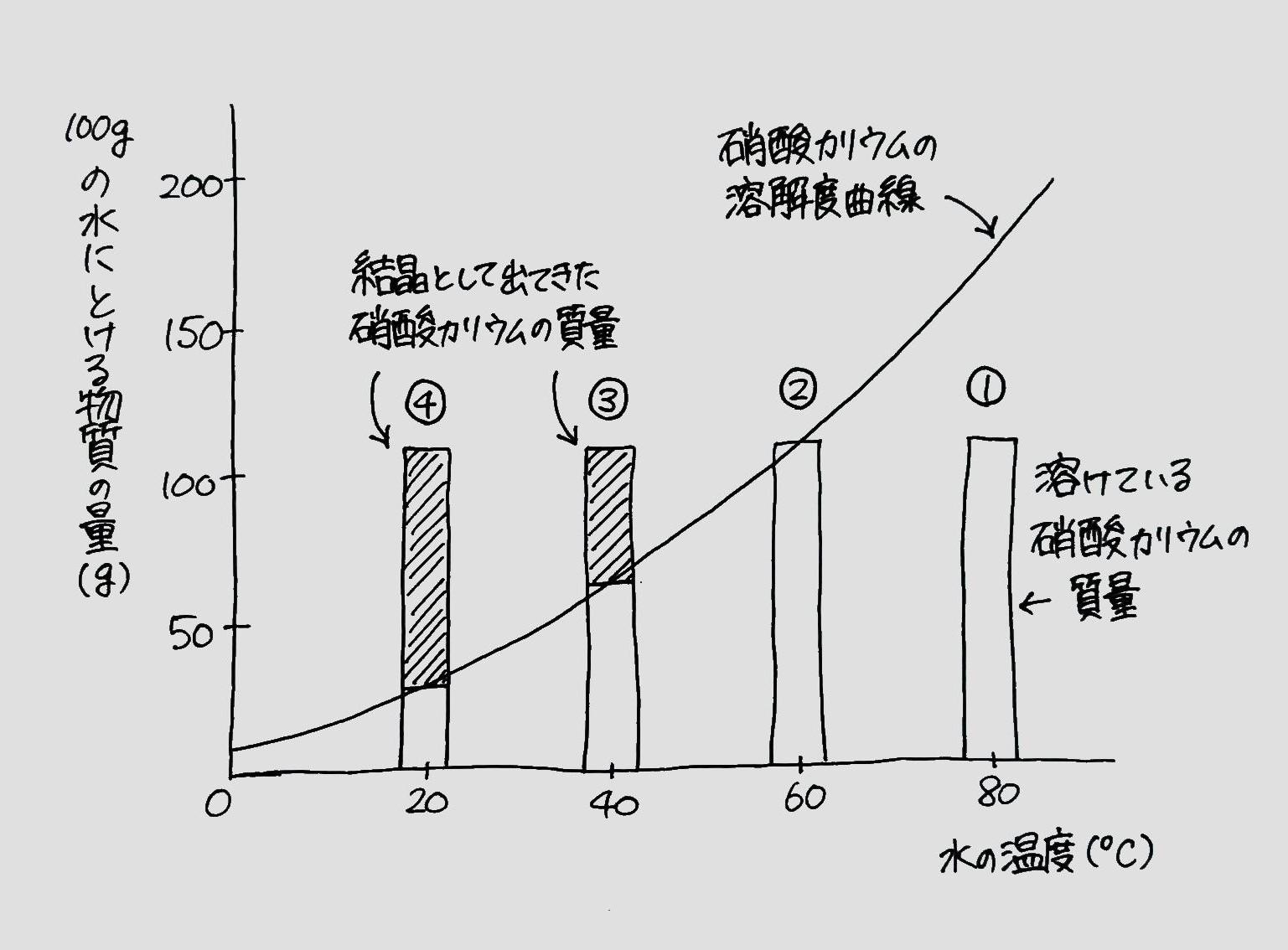 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 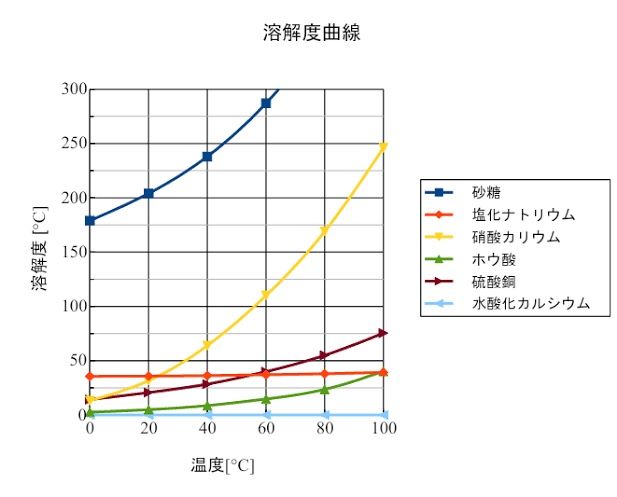 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 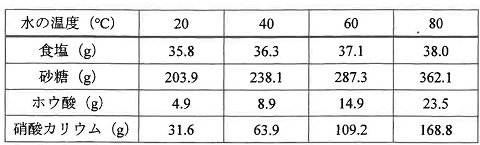 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note | 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
 12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |  12 水に溶ける 量 について 高校化学 休校課題はこちらから Note |
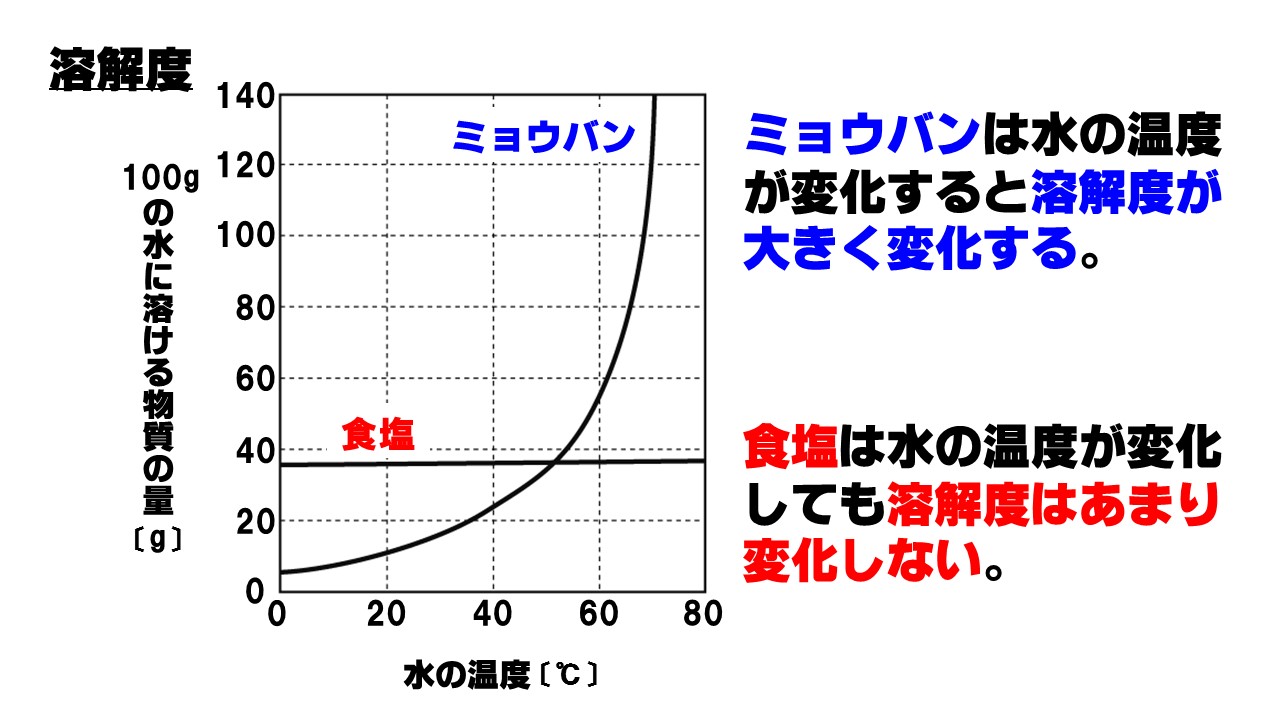
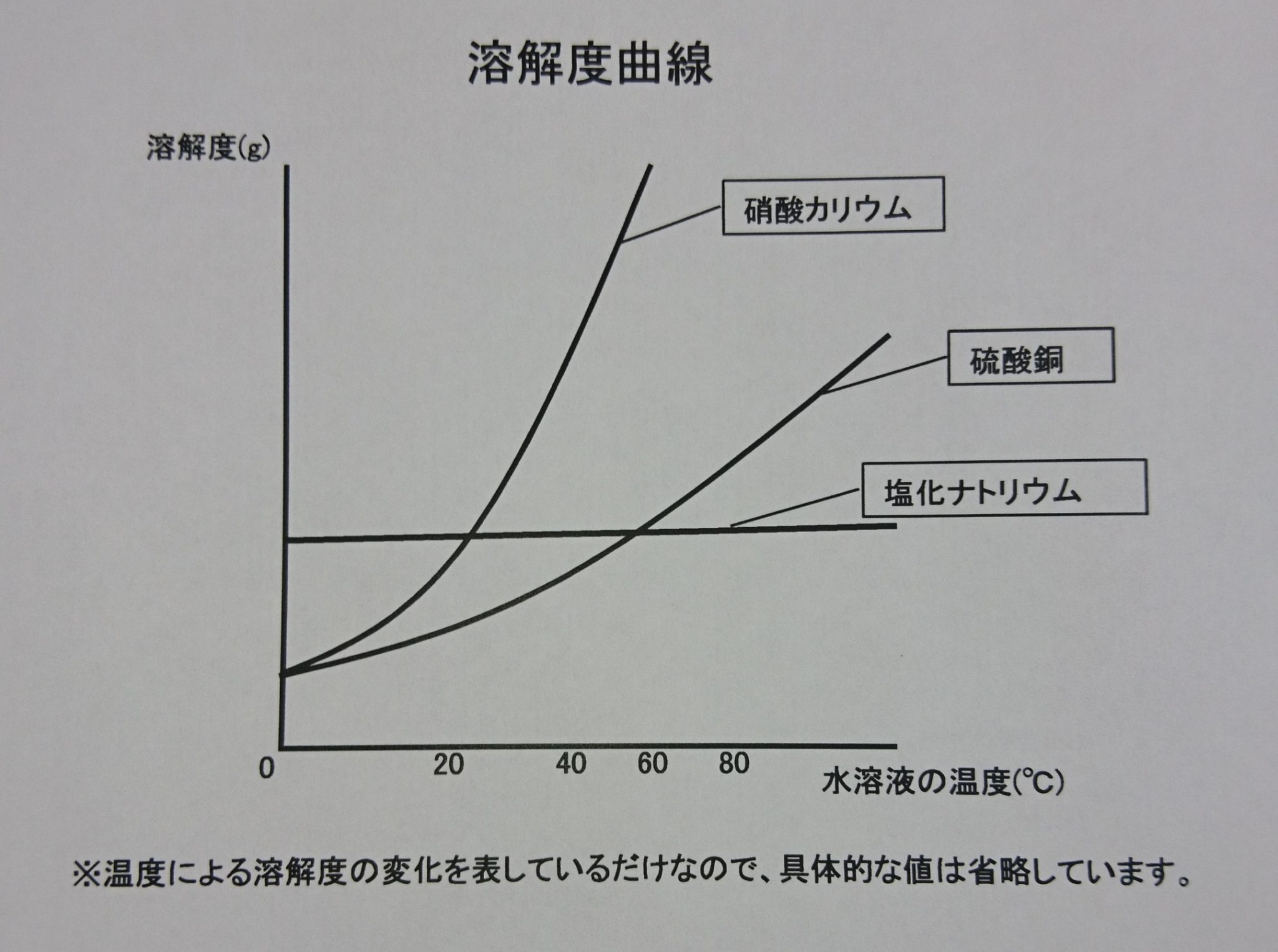
質量パーセント濃度 ・・・溶液全体のうち、どのくらいの割合で溶質が溶けているのか 飽和水溶液 ・・・飽和に達した水溶液 飽和 ・・・もうそれ以上、溶質が溶けなくなった状態 溶 2 溶解度(ようかいど)とは ① 溶解度 溶解度 100g の水にとける物質の質量のこと。 溶解度は温度で変わる 水にとける物質には、砂糖(ショ糖)、食塩、ミョウバンなどがあります
コメント
コメントを投稿